En la Unidad de Cuidados Intensivos Pediátricos (UCIP), los pacientes con diabetes mellitus tipo 1 (DM1) ingresan principalmente por cetoacidosis diabética (CAD) al debut de la enfermedad o en descompensaciones de la misma, siendo esta la principal causa de hospitalización y mortalidad en niños con este trastorno metabólico (1).
Cuando ingresa un paciente con esta problemática en la UCIP, habitualmente presenta deshidratación, síntomas respiratorios (taquipnea, patrón respiratorio de Kussmaul), digestivos (náuseas, vómitos y/o dolor abdominal), y neurológicos (confusión y bajo nivel de consciencia); que serán más o menos críticos en función de la gravedad de la cetoacidosis.
La prioridad del equipo asistencial es estabilizar al paciente, rehidratar, corregir las alteraciones electrolíticas y disminuir la glucemia de forma progresiva y controlada (una bajada brusca podría derivar en complicaciones graves, como el edema cerebral). Para ello es esencial una monitorización estricta de los niveles de glucosa y otros parámetros alterados relacionados, como los iones y los cuerpos cetónicos. Hasta el momento estos se obtenían únicamente de muestras sanguíneas que extrae enfermería con procedimientos mínimamente invasivos (punción capilar o venosa) y generando cierta molestia al paciente. Estas determinaciones, que en las primeras 24 horas de ingreso son continuadas (habitualmente de manera horaria) implican un mínimo de 24 punciones a un niño, que ya se encuentra en un entorno desconocido y hostil y con un estado clínico afectado, dificultando la relación enfermera-paciente. Además, aunque estas técnicas aportan información de gran importancia que permite tomar decisiones clínicas, no muestran la dinámica de la glucosa, porque solo proporcionan información puntual y estática en el momento de la medición.
LA PRIORIDAD DEL EQUIPO ASISTENCIAL ES ESTABILIZAR AL PACIENTE, REHIDRATAR, CORREGIR LAS ALTERACIONES ELECTROLÍTICAS Y DISMINUIR LA GLUCEMIA DE FORMA PROGRESIVA Y CONTROLADA
En los últimos años, se ha producido un importante desarrollo tecnológico en el manejo de la diabetes donde destacan los sistemas de monitorización continua de glucosa (MCG) que nos permiten conocer mejor el comportamiento y variabilidad de la glucosa. Dichos dispositivos son capaces de obtener la glucosa intersticial mediante un filamento flexible que es insertado debajo de la piel de forma mínimamente invasiva. Presentan un papel importante en la gestión de la diabetes en el ámbito ambulatorio desde hace años, donde demostraron que reducen el número de episodios de hipoglucemia, y mejoran el control glucémico y la calidad de vida de los pacientes (y sus cuidadores), inicialmente en DM1, y actualmente extensivo a la diabetes tipo 2. A nivel hospitalario, su uso surge con la llegada del COVID-19, cuando la asistencia era masiva y los equipos de protección individual (EPIS) escaseaban, el uso de los sensores suponía minimizar el contacto con pacientes infectados y mantener el control glucémico de los mismos; motivo por el cual la Administración de Alimentos y Medicamentos (Food and Drugs Administration o FDA), permitió el uso de dichos dispositivos en el paciente hospitalizado durante la pandemia (2).
Debido a esto, la mayoría de la bibliografía existente de la MCG en el ámbito hospitalario se centra en pacientes adultos con diabetes, en tratamiento con insulina intravenosa en perfusión continua. Sin embargo, surgen ya algunas publicaciones que dejan ver el potencial de esta tecnología, no sólo en el paciente con diabetes, sino en otros perfiles de pacientes: críticos, en contexto perioperatorio, en relación con la recuperación tras sufrir un ictus o infarto. En todos estos escenarios, disminuir la variabilidad glucémica (es decir, las oscilaciones producidas por subidas y bajadas de los niveles de glucosa) ha demostrado ser un factor importante en la reducción de tiempos de ingreso y disminución de la mortalidad, llegando a hablarse de la posibilidad de que se convierta en la quinta constante a monitorizar en el paciente crítico (3,4,5,6,7).
Por todo esto, y aunque a día de hoy sigue sin regularse su uso y no se dispone de directrices de consenso sobre las cifras objetivo de MCG en hospital, algunas de las principales guías de práctica clínica lo contemplan con limitaciones: la Endocrine Society, refiere que debería emplearse en pacientes no críticos con riesgo de hipoglucemia, asociando su uso con glucemias capilares; la American Diabetes Association (ADA) solo en personas con diabetes que disponen de él en su domicilio y, aunque se encuentren hospitalizadas, sean competentes para usarlos; y otras guías, como la Society of Critical Care Medicine, no mencionan los sensores, pero sí la recomendación de una monitorización estrecha y constante ante perfusiones continuas de insulina. Ante este escenario, podemos ver que los sensores de MCG mantienen un uso casi anecdótico a nivel hospitalario y que todavía tienen que demostrar su beneficio, por lo que debemos generar evidencia en este aspecto (7,8,9,10).
Pero como en todo, la pediatría, por las peculiaridades éticas de la investigación con niños, sigue a la cola en estudios y publicaciones que extrapolen estos datos a este ámbito de actuación. En este campo, las pocas publicaciones existentes centran su atención en el mismo foco: la cetoacidosis diabética, el enemigo número uno en niños y adolescentes con diabetes. Los pocos trabajos existentes consisten en estudios retrospectivos que concluyen que el uso de los sensores de MCG es factible y preciso y que, a pesar de que la gravedad de la cetoacidosis disminuye la precisión de las determinaciones obtenidas por este dispositivo, su uso es seguro y efectivo clínicamente. Por ello, sugieren que podrían ser útiles para valorar tendencias y detectar valores anormales, aunque se necesitan estudios más grandes y de mayor calidad metodológica (1,11).
Paralelamente en la UCI Pediátrica del Hospital Clínico de Santiago de Compostela, hace tres años, también nos preguntamos ¿por qué no colocamos un sensor en la UCI Pediátrica desde el debut? Con el claro objetivo de ofrecer un control glucémico estricto y riguroso, sin olvidarnos de prestar cuidados humanizados de calidad, incorporamos en nuestro Protocolo de Manejo de Cetoacidosis Diabética del año 2021, la colocación del sensor de MCG como parte esencial en el manejo del debut de la diabetes.
CUANDO INGRESA UN PACIENTE QUE ACABA DE DEBUTAR, SE LE COLOCA EL SENSOR DE MONITORIZACIÓN CONTINUA DE GLUCOSA RECOGIDO EN LA CARTERA DE SERVICIOS DE NUESTRO SISTEMA SANITARIO
Cuando ingresa un paciente que acaba de debutar, se le coloca el sensor de monitorización continua de glucosa recogido en la cartera de servicios de nuestro sistema sanitario (inicialmente Freestyle libre 2® y en la actualidad Freestyle libre 3®). Según el protocolo elaborado en nuestra unidad, durante las primeras horas de ingreso, se recogerán muestras sanguíneas capilares o venosas de manera horaria o en horas alternas (en base a la gravedad de la cetoacidosis en el momento de ingreso), para obtener las determinaciones de glucemia y cetonemia. Paralelamente, se recogen los datos de glucemia y tendencia del sensor, los cuales serán registrados por enfermería de manera horaria, excepto en caso de alerta por hiper o hipoglucemia, que se verificará con glucemia capilar en el momento.
A lo largo de estos tres años, el sensor ha sido colocado a 19 pacientes que ingresaron con diagnóstico de cetoacidosis diabética como manifestación del debut de DM1, y la percepción por parte del equipo de enfermería es unánime: “un alto grado de aceptación, destacando la seguridad del paciente y la mejora de la calidad asistencial”. Como en cualquier equipo humano, son pocos los cambios exentos de discrepancias, o la introducción de nuevos materiales o técnicas sin generar debates internos, por eso sorprende la insólita respuesta por parte del equipo, que coincidimos al 100% en que el uso de los sensores supone un salto de calidad en nuestra asistencia.
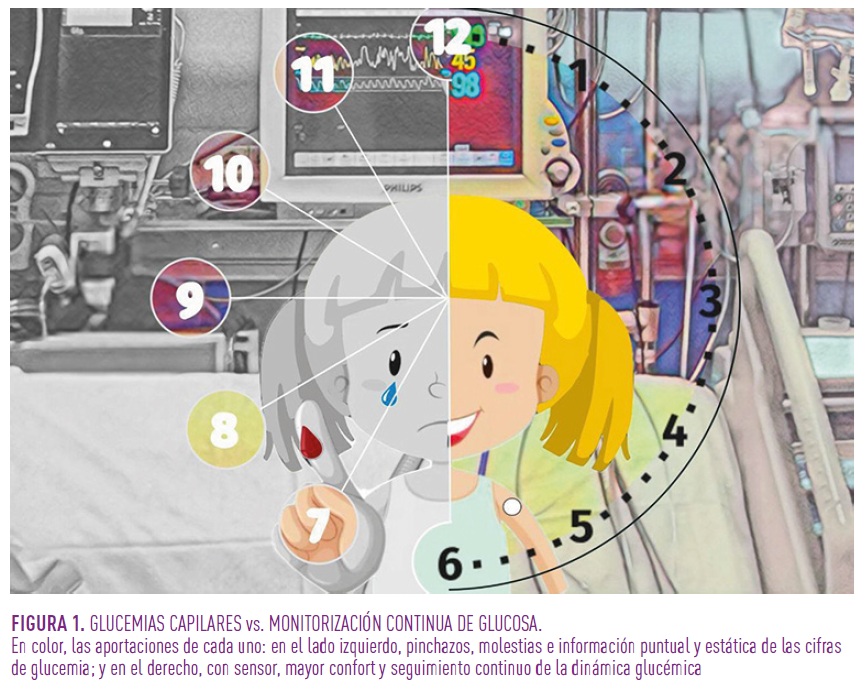
En cuanto a las ventajas en la monitorización y el tratamiento, al comparar los valores de glucemias capilares con las del sensor de MCG en el mismo período, y la falta de la publicación de los resultados, nuestra impresión es que la tendencia es paralela; basta con revisar una gráfica de registro de enfermería para ver que una alerta de hipoglucemia en el sensor se corrobora en mayor o menor medida con una hipoglucemia capilar. Además, el cambio es sustancial: es como comparar “24 fotos” de la glucemia de nuestro paciente (número de pinchazos capilares que se realizarían), con un vídeo en directo de su variabilidad glucémica (MCG). Esto ofrece un mayor control de las tendencias, aportándonos una valiosa información anticipatoria que facilita la toma de decisiones clínicas más precoces y permite espaciar las glucemias capilares, especialmente en horario nocturno. Pero las ventajas se extienden más allá del control exhaustivo: a las enfermeras nos define la palabra cuidar, y poder reducir los pinchazos y respetar el horario de sueño mejora la atención humanizada y facilita una buena relación enfermera-paciente (ambas ventajas, se plasman en la imagen adjunta) Figura1. Es esta parte, la que más perciben y valoran el paciente y su familia, transmitiéndonos su satisfacción con el uso de esta nueva tecnología.
Sobre la enfermería, especialmente de endocrino y atención primaria, recae la formación del paciente y la familia para el autocuidado y manejo de su patología. Pero esta educación terapéutica comienza en nuestra UCIP; es nuestra labor enseñar la técnica correcta para la realización de diferentes procedimientos (medición de glucemia capilar, la administración de insulina, etc.), y ahora también el uso del sensor. Entendemos que su uso desde el ingreso facilita el aprendizaje y la adaptación.
La incorporación del sensor en nuestra práctica clínica ha dejado patente la necesidad de formarnos para poder aprovechar las ventajas que nos ofrece la MCG, de lo contrario, esto supondría la limitación más importante en el uso de esta nueva tecnología; ya que aporta muchos datos que debemos registrar ordenadamente y saber interpretar para anticiparnos y evitar complicaciones graves. Además, conocer en profundidad las funcionalidades de esta tecnología es clave para llevar a cabo una buena educación terapéutica.
Una de las tareas pendientes, en base a las recomendaciones realizadas por el Consenso Internacional de Expertos en Diabetes, y que también hemos detectado a nivel asistencial, es el uso de sensores duales. Estos aportarían la monitorización continua de glucosa y cetona, reduciendo las determinaciones capilares repetidas de ambos parámetros. Esperamos que sea factible en un futuro próximo.
CONCLUSIONES
Todo lo expuesto deja patente nuestra satisfacción con el uso de los sensores de MCG en el manejo de la cetoacidosis diabética en la UCIP. A lo largo de estos tres años nos mostraron su utilidad clínica, ayudándonos en nuestro reto de ofrecer un control glucémico estricto y riguroso y proporcionando cuidados humanizados de calidad. Sin embargo, somos conscientes de la necesidad de estudios que avalen nuestra experiencia y que esperamos resulten de interés en nuestro campo de actuación.
BIBLIOGRAFÍA
- Park E, Kim M. Clinical use of continuous glucose monitoring in critically ill pediatric patients with diabetic ketoacidosis. Diabetes technology. August 2023; 25(8):529-537. doi: 10.1089/dia.2023.0012. Epub Jul 17, 2023. PMID: 37155338; PMCID: PMC10387156.
- Yao Y, Zhao YH, Zheng WH, Huang HB. Continuous subcutaneous glucose monitoring in critically ill patients during insulin treatment: a meta-analysis. Am J Transl Res. 2022 Jul 15; 14(7):4757-4767. PMID: 35958452; PMCID: PMC9360883.
- Grupo de Trabajo de Tecnologías Aplicadas a la Diabetes. Guía Rápida de Uso. Monitorización Continua de Glucosa y Monitorización Flash de Glucosa. Sociedad Española de Diabetes (SED); 2018. chrome-extension://efaidnbmnnnibpcajpcglclefindmkaj/https://www.sediabetes.org/wp-content/uploads/monitorizacion-continua-y-flash-glucosa.pdf (acceso el 12 noviembre 2024).Pott T, Jimenez-Vega J, Parker J, Fitzgerald R. Continuous Glucose Monitoring in Pediatric Diabetic Ketoacidosis. J Diabetes Sci Technol. 2024 Jul;18(4):899-903. doi: 10.1177/19322968221140430. Epub 2022 Nov 23. PMID: 36416103; PMCID: PMC11307226.
- U.S. Food and Drug Administration. Enforcement Policy for Non-Invasive Remote Monitoring Devices Used to Support Patient Monitoring During the Coronavirus Disease 2019 (COVID-19) Public Health Emergency (Actualización Marzo 2023) 2020. Disponible en: https://www.fda.gov/media/136290/download
- Bhargavi Patham, Abhishek Kansara, Archana R. Sadhu; Real-time Continuous Glucose Monitoring in the Intensive Care Unit: The Fifth Vital Sign. Diabetes Care 20 May 2024; 47 (6): 924–926.
- Palaiodimou L, Lioutas VA, Lambadiari V, Theodorou A, Themistocleous M, Aponte L, Papagiannopoulou G, Foska A, Bakola E, Quispe R, Mendez L, Selim M, Novak V, Tzavellas E, Halvatsiotis P, Voumvourakis K, Tsivgoulis G. Glycemic variability of acute stroke patients and clinical outcomes: a continuous glucose monitoring study. Ther Adv Neurol Disord. 2021 Sep 22;14:17562864211045876. doi: 10.1177/17562864211045876. PMID: 34589140; PMCID: PMC8474316.
- Avari P, Lumb A, Flanagan D, Rayman G, Misra S, Dhatariya K, Choudhary P. Continuous Glucose Monitoring Within Hospital: A Scoping Review and Summary of Guidelines From the Joint British Diabetes Societies for Inpatient Care. J Diabetes Sci Technol. 2022 Nov 28:19322968221137338. doi: 10.1177/19322968221137338. Epub ahead of print. PMID: 36444418.
- Korytkowski MT, Muniyappa R, Antinori-Lent K, Donihi AC, Drincic AT, Hirsch IB, Luger A, McDonnell ME, Murad MH, Nielsen C, Pegg C, Rushakoff RJ, Santesso N, Umpierrez GE. Management of Hyperglycemia in Hospitalized Adult Patients in Non-Critical Care Settings: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2022 Jul 14;107(8):2101-2128. doi: 10.1210/clinem/dgac278. PMID: 35690958; PMCID: PMC9653018
- ElSayed NA, Aleppo G, Aroda VR, Bannuru RR, Brown FM, Bruemmer D, Collins BS, Hilliard ME, Isaacs D, Johnson EL, Kahan S, Khunti K, Leon J, Lyons SK, Perry ML, Prahalad P, Pratley RE, Seley JJ, Stanton RC, Gabbay RA, on behalf of the American Diabetes Association. 7. Diabetes Technology: Standards of Care in Diabetes-2023. Diabetes Care. 2023 Jan 1;46(Suppl 1):S111-S127. doi: 10.2337/dc23-S007. PMID: 36507635; PMCID: PMC9810474.
- Honarmand K, Sirimaturos M, Hirshberg EL, Bircher NG, Agus MSD, Carpenter DL, Downs CR, Farrington EA, Freire AX, Grow A, Irving SY, Krinsley JS, Lanspa MJ, Long MT, Nagpal D, Preiser JC, Srinivasan V, Umpierrez GE, Jacobi J. Society of Critical Care Medicine Guidelines on Glycemic Control for Critically Ill Children and Adults 2024. Crit Care Med. 2024 Apr 1;52(4):e161-e181. doi: 10.1097/CCM.0000000000006174. Epub 2024 Jan 19. PMID: 38240484.
- Pott T, Jimenez-Vega J, Parker J, Fitzgerald R. Continuous Glucose Monitoring in Pediatric Diabetic Ketoacidosis. J Diabetes Sci Technol. 2024 Jul;18(4):899-903. doi: 10.1177/19322968221140430. Epub 2022 Nov 23. PMID: 36416103; PMCID: PMC11307226.







