El crecimiento es un fenómeno biológico que transcurre desde la concepción hasta el final de la pubertad, alcanzando entonces la talla adulta. Durante el crecimiento el individuo incrementará su masa corporal, adquiriendo la madurez física y psicológica. La talla adulta de un individuo está influenciada por factores genéticos y hormonales. De entre estos últimos, destacar el eje de hormona de crecimiento y factores de crecimiento (“GH/IGF-1”), en el que la hormona de crecimiento (GH) antehipofisaria, actúa directamente sobre el hueso e indirectamente sobre sus receptores en el hígado (GHR), estimulando la producción de factores periféricos (factor de crecimiento similar a la insulina-1 (IGF-1), proteína transportadora del factor de crecimiento similar a la insulina 3 (IGFBP-3) y unidad ácido lábil (ALS). Además, en el crecimiento influyen muchos aspectos como: la nutrición, la pubertad, el sueño, el entorno psicosocial, la actividad física, los hábitos de vida saludables, así como la exposición a fármacos/tóxicos. Una enfermedad crónica y, especialmente un mal control de la misma, impactan negativamente sobre el patrón de crecimiento. En consecuencia y, de acuerdo con la Organización Mundial de la Salud, el crecimiento es el mejor indicador del estado de salud y bienestar de los niños y adolescentes.
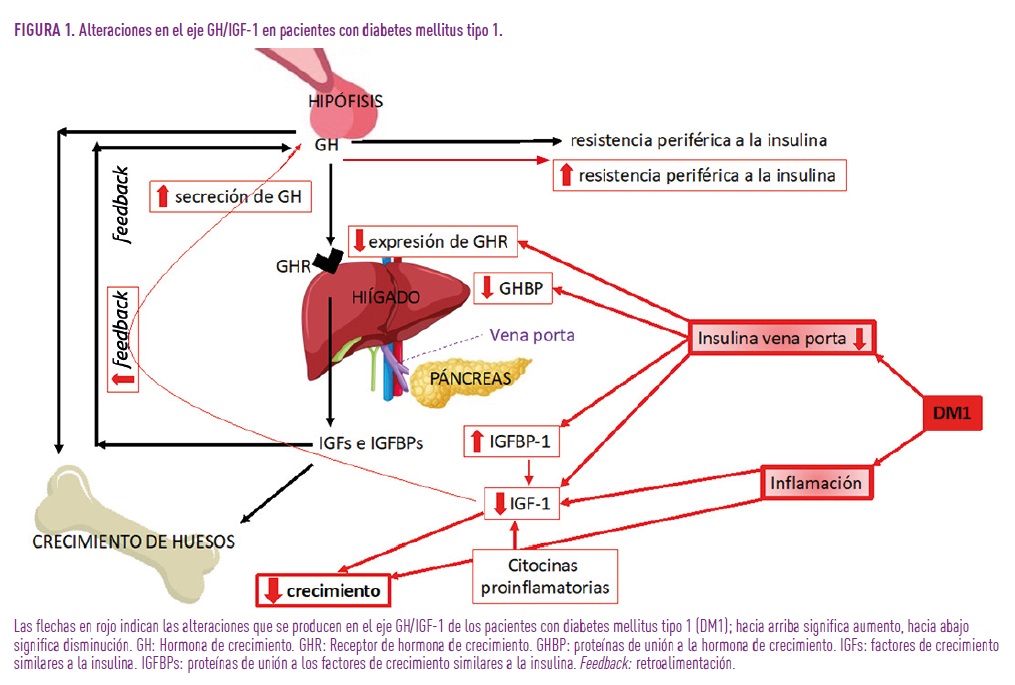
La insulina desempeña una función esencial en la fisiología del crecimiento normal, al regular el eje de crecimiento GH/IGF-1. De hecho, la secreción normal de insulina y sus niveles adecuados en la circulación de la vena porta (que transporta la sangre desde intestino, bazo, páncreas y vesícula biliar hasta el hígado), son indispensables para obtener concentraciones en sangre normales de IGF-1 y proteínas de unión a IGFs (IGFBPs). Además, varios estudios han demostrado que la insulina estimula la expresión del receptor de GH (GHR) en el hígado, aumenta la disponibilidad de estos receptores celulares, y promueve la señalización post-receptor de GH, regulando así la síntesis en el hígado de IGF-1 e IGFBPs. La Figura 1 muestra esquemáticamente los factores hormonales del eje de crecimiento, así como las alteraciones encontradas en pacientes con diabetes mellitus tipo 1 (DM1).
En la DM1, el crecimiento lineal se puede ver afectado negativamente en relación con varios factores, como la duración de la enfermedad y el control metabólico deficiente, que serán expuestos a continuación.
Algunos estudios han demostrado correlación entre la duración de la DM1 y la talla adulta, con peor crecimiento en pacientes con una diabetes de mayor evolución. En este sentido, la tasa de crecimiento parece estar influenciada por la edad de inicio de la DM1, produciéndose el deterioro del crecimiento más grave en niños a los que se les diagnostica la enfermedad en la primera infancia. Varios estudios han demostrado que los niños con DM1 presentan una reducción en las desviaciones estándar de altura y en la velocidad de crecimiento después del inicio de la enfermedad durante la edad prepuberal. Si bien algunos investigadores no mostraron la influencia del control metabólico en el crecimiento puberal en pacientes con DM1, otros han demostrado que los niveles altos de hemoglobina glicosilada (HbA1c) y el control glucémico deficiente se correlacionan con un crecimiento reducido en altura en adolescentes con DM1. Las investigaciones sobre el deterioro del estirón puberal comparando adolescentes de sexo femenino versus masculino, muestran resultados contradictorios. Por otra parte, Bizzarri et al. demostraron que la velocidad de crecimiento después del diagnóstico de DM1 estaba directamente asociada con la actividad residual de las células beta pancreáticas, evaluada como niveles de péptido C.
LA INSULINA DESEMPEÑA UNA FUNCIÓN ESENCIAL EN LA FISIOLOGÍA DEL CRECIMIENTO NORMAL, AL REGULAR EL EJE DE CRECIMIENTO GH/IGF-1
La altura en el momento del diagnóstico de DM1 en niños es un tema debatido en la literatura. Muchos estudios constataban que los niños al inicio de la DM1 eran más altos que sus pares sin diabetes, mientras que otros autores no han confirmado estos datos. La hipótesis “aceleradora” sugiere que el aumento de las tasas de crecimiento y el exceso de adiposidad conducen a la resistencia a la insulina, promoviendo hiperfunción de células beta y aumento de la expresión de antígenos, lo que en última instancia conduciría a autoinmunidad y aceleración del fallo de células beta. Además, muchos trabajos recientes han confirmado que un rápido aumento de altura, peso e índice de masa corporal en la primera infancia parece estar relacionado con el desarrollo de la autoinmunidad de los islotes y con la posterior aparición de DM1 en los niños.
Un control metabólico deficiente en niños con DM1 se correlaciona con afectación del crecimiento lineal. Diversos autores han detectado una asociación entre los niveles más bajos de IGF-1 en aquellos niños con niveles más altos de HbA1c. El control glucémico deficiente en la DM1 también se asocia con la resistencia de los tejidos a la acción de la GH. Un ejemplo extremo de cómo el control diabético deficiente impacta negativamente el crecimiento es el síndrome de Mauriac. Este síndrome, caracterizado por retraso del crecimiento, detención de la pubertad y hepatomegalia con alteración de los lípidos, constituye la afección más crítica relacionada con el crecimiento, caracterizada por DM1 de larga evolución y mal controlada en relación con una insulinización crónica desfavorable. Esta disminución en el crecimiento lineal parece deberse en parte a una reducción en la capacidad de respuesta de la GH, lo que lleva a niveles bajos del IGF-1. Afortunadamente, en nuestro país, dados los medios accesibles de control de DM1, es excepcional hallar casos de síndrome de Mauriac y, por ende, tanta afectación de la talla. Finalmente, un mal control metabólico también contribuye a un retraso en el inicio y/o progresión de la pubertad, pudiendo traducirse en un estirón puberal subóptimo con impacto en la talla final.
En niños con DM1, la deficiencia de insulina en vena porta ocurre con frecuencia y determina la hipersecreción de GH, bajas concentraciones circulantes de IGF-1 e IGFBP-3, con niveles elevados en sangre de IGFBP-1 en consecuencia. Los niveles elevados de IGFBP-1 podrían, además, inhibir la fracción libre bioactiva de IGF-1 (la que actúa realmente en los tejidos diana). También se ha descrito que los niveles bajos de IGF-1 aumentan la retroalimentación negativa a la glándula hipofisaria y producen hipersecreción de GH, el factor más importante que contribuye a la resistencia a la insulina durante la pubertad en adolescentes con DM1. Las proteínas de unión a la GH (GHBPs) se forman por la escisión proteolítica del GHR transmembrana, y los niños con DM1 presentan niveles bajos de GHBP secundarios a niveles bajos de insulina portal.
UN CONTROL METABÓLICO DEFICIENTE EN NIÑOS CON DM1 SE CORRELACIONA CON AFECTACIÓN DEL CRECIMIENTO LINEAL
Adicionalmente, el crecimiento subóptimo en la población con DM1 probablemente refleja un trastorno metabólico contínuo relacionado con las complicaciones microvasculares clásicas de la diabetes, particularmente la nefropatía diabética. Se ha descrito que los pacientes con DM1 tienen marcadores inflamatorios circulantes elevados, incluidos las interleucinas-1beta, 6 y 8 así como del factor de necrosis tumoral alfa, la proteína C reactiva y el fibrinógeno. Estas y otras citocinas proinflamatorias pueden afectar el crecimiento tanto por efectos directos sobre la placa de crecimiento de los huesos como por la supresión local de las acciones de IGF-1 al producir resistencia a la acción de IGF-1 o disminuir sus niveles en sangre.
De forma similar, la variabilidad de la glucosa afecta fuertemente el riesgo de complicaciones microvasculares y macrovasculares relacionadas con la diabetes. La variabilidad glucémica se correlaciona con el crecimiento lineal en niños con DM1, de tal manera que se han publicado índices de variabilidad glucémica bajos en los niños con los percentiles de altura más altos.
Por lo anteriormente expuesto, mejorar el control glucémico puede conducir a mejores niveles de IGF-1, menor resistencia de los tejidos a la acción de la GH y, en consecuencia, mejorar el crecimiento lineal.
Otros factores asociados con un crecimiento lineal deficiente en la DM1 incluyen la adición de otra enfermedad no adecuadamente controlada (por su frecuente asociación, la enfermedad celíaca), así como las transgresiones de la dieta. Como en otras enfermedades crónicas, los pacientes con DM1 también son más susceptibles a presentar trastornos del comportamiento alimentario, con su efecto detrimental sobre el desarrollo puberal y el crecimiento longitudinal. Algunos estudios apuntan a que las cada vez más populares dietas muy bajas en hidratos de carbono, si no se emplean cuidadosamente, pueden aumentar el riesgo de un crecimiento lineal atenuado en individuos con DM1.
En los últimos años, a pesar de los avances tecnológicos en el tratamiento de la DM1, hay resultados contradictorios en la literatura sobre su efecto en el crecimiento y la talla adulta. Esta discrepancia entre estudios puede deberse a la metodología empleada, duración del diagnóstico, la población de estudio y control, incluyendo diferencias étnicas y en el nivel socioeconómico. La terapia convencional con insulina subcutánea no parece capaz de reemplazar la secreción de insulina pancreática en la circulación de la vena porta. Aunque algunos estudios han demostrado un aumento de los niveles en sangre de IGF-1 tras la mejora de la terapia intensiva con insulina, alcanzando altura final normal o ligeramente reducida a la de sus pares no afectados, el uso de terapia con infusión subcutánea continua de insulina (ISCI) tampoco parece mejorar la hipoinsulinización hepática crónica y no parece influir en el patrón de crecimiento lineal en comparación con la terapia de múltiples inyecciones diarias (MDI). En un interesante estudio de Hainaire-Broutin et al. se evaluó el eje GH/IGF-1 en pacientes con DM1 en tratamiento con insulina subcutánea convencional frente a ISCI y aunque los sujetos en ISCI tenían una HbA1c más baja comparada con el grupo en terapia convencional, no había diferencia en los niveles de GHBP. A los pacientes que recibieron ISCI se les administró a continuación una infusión portal continua de insulina (IPCI) a través de una bomba implantable. Aunque no hubo diferencias significativas en la HbA1c entre la ISCI y la IPCI, se produjo un mayor aumento de la GHBP, una casi normalización de la IGF-1, y normalización de IGFBP-3. Posteriormente, otros autores también han confirmado resultados similares sobre los efectos beneficiosos de la terapia IPCI sobre el eje GH/IGF-1. Estos resultados sugieren que no es únicamente el control glucémico lo que influye en el eje GH/IGF-1 en la DM1, sino que la presencia de cantidades incluso bajas de insulina residual en la circulación portal, son determinantes para el funcionamiento del eje GH/IGF-1. Queda por determinar si es factible la implementación de la terapia IPCI en la DM1.
En los últimos años se han descubierto otros factores circulantes en sangre del eje periférico GH/IGF-1, denominados papalisinas y estaniocalcinas, cuyo estudio en niños con DM1 puede ayudar a entender el impacto de la enfermedad en el crecimiento de estos niños.
CONCLUSIÓN: A pesar de los avances en el conocimiento del eje GH/IGF-1, aún persisten muchas dudas sobre su afectación en el caso de enfermedades, incluyendo la diabetes mellitus tipo 1. Existen datos contradictorios sobre el impacto en el crecimiento y talla adulta de las terapias con régimen intensivo de insulina, sugiriendo persistencia de anomalías bioquímicas en el eje GH/IGF-1 en niños con DM1, aunque parecen alcanzar una talla adulta normal o similar a la de su población de referencia.
BIBLIOGRAFÍA
- Bizzarri C, Timpanaro TA, Matteoli MC, Patera IP, Cappa M, Cianfarani S. Growth Trajectory in Children with Type 1 Diabetes Mellitus: The Impact of Insulin Treatment and Metabolic Control. Horm Res Paediatr. 2018; 89(3):172-177
- Cianfarani S, Bonfanti R, Bitti ML, et al. Growth and insulin-like growth factors (IGFs) in children with insulin-dependent diabetes mellitus at the onset of disease: Evidence for normal growth, age dependency of the IGF system alterations, and presence of a small (approximately 18-kilodalton) IGF-binding protein-3 fragment in serum. J Clin Endocrinol Metab. 2000; 85: 4162–4167
- Muñoz MT, Barrios V, Pozo J, Argente J. Insulin-like growth factor I, its binding proteins 1 and 3, and growth hormone-binding protein in children and adolescents with insulin-dependent diabetes mellitus: Clinical implications. Pediatr Res. 1996; 39: 992–998
- Koren D. Growth and development in type 1 diabetes. Curr Opin Endocrinol Diabetes Obes. 2022; 29(1):57-64
- Waden J, Forsblom C, Thorn LM, et al. Adult stature and diabetes complications in patients with type 1 diabetes: the FinnDiane Study and the diabetes control and complications trial. Diabetes. 2009; 58(8):1914–1920
- Snell-Bergeon JK, West NA, Mayer-Davis EJ, et al. Inflammatory markers are increased in youth with type 1 diabetes: the SEARCH Case-Control study. J Clin Endocrinol Metab. 2010; 95(6): 2868–2876
- Marcovecchio ML, Heywood JJ, Dalton RN, Dunger DB. The contribution of glycemic control to impaired growth during puberty in young people with type 1 diabetes and microalbuminuria. Pediatr Diabetes. 2014;15(4):303–308
- Hanaire-Broutin H, Sallerin-Caute B, Poncet MF, et al. Insulin therapy and GH- IGF-I axis disorders in diabetes: impact of glycaemic control and hepatic insulinization. Diabetes Metab. 1996; 22: 245–250.
- Shishko PI, Dreval AV, Abugova IA, Zajarny IU, Goncharov VC. Insulin-like growth factors and binding proteins in patients with recent-onset type 1 (insulin-dependent) diabetes mellitus: influence of diabetes control and intraportal insulin infusion. Diabetes Research and Clinical Practice. 1994; 25: 1–12
- Bereket A, Lang CH, Blethen SL, Ng LC, Wilson TA. Insulin treatment normalizes reduced free insulin-like growth factor-I concentrations in diabetic children. Clin Endocrinol. (Oxf.) 1996;45:321–326
- Martín-Rivada Á, Guerra-Cantera S, Campillo-Calatayud A, et al. Pappalysins and Stanniocalcins and Their Relationship With the Peripheral IGF Axis in Newborns and During Development. J Clin Endocrinol Metab. 2022;107(10):2912-2924.







