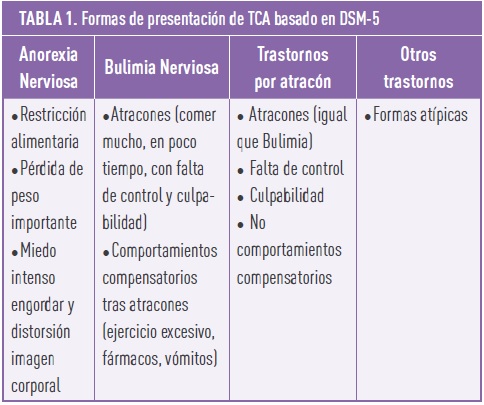
Los trastornos de la conducta alimentaria (TCA) son un grupo de enfermedades mentales que afectan fundamentalmente a adolescentes y adultos jóvenes que conllevan a una mayor utilización de recursos sanitarios y costes, y sobre todo a una peor calidad de vida y una alta tasa de mortalidad. La prevalencia en los últimos años ha ido en aumento no solo por un mayor número de casos, sino también por una mayor detección al incluir en el Manual de diagnóstico de salud mental (DSM-5) el trastorno por atracón como un TCA (Tabla 1). Se han descrito múltiples factores de riesgo para el desarrollo de los TCA. El “modelo interactivo de influencias biopsicosociales” explica la aparición de los TCA interrelacionando factores genéticos y familiares, factores psicológicos (rasgos de personalidad como perfeccionismo o autoexigencia, insatisfacción corporal, baja autoestima, ideal de delgadez) así como factores relacionados con actividades y profesiones (deportistas, modelos etc.) o la presencia de enfermedades crónicas dónde la dieta forma parte del tratamiento como la Diabetes Mellitus tipo 1(DM1), la celiaquía, fibrosis quística o el síndrome intestino irritable.
Es conocido que los jóvenes con DM1 tienen una peor salud mental que sus iguales sin diabetes. Convivir con esta enfermedad crónica puede conducir a la aparición de cuadros de ansiedad e incluso se ha observado un mayor riesgo de sufrir depresión clínicamente significativa. No solo se han descrito altas tastas de depresión y ansiedad (11 y 21% respectivamente), sino también un riesgo muy elevado de desarrollar un trastorno alimentario (siglas del inglés T1DE). Se estima que entre el 10-30% de las mujeres con DM1 tendrán un trastorno alimentario frente a alrededor del 4% en la población general. Las personas con DM1, desde el diagnóstico, establecen un vínculo entre la insulina y el aumento de peso. La pérdida de peso significativa es un síntoma cardinal del debut y, por otro lado, la dieta constituye uno de los pilares del tratamiento. Si añadimos a esto, el impacto que produce el diagnóstico de la propia enfermedad, especialmente durante la adolescencia, no debería resultar extraño que la diabetes se asocie a un aumento de la incidencia de TCA.
Los T1DE pueden presentarse como anorexia (AN) o bulimia nerviosa (BN), como un trastorno por atracón (TA) o como un trastorno llamado diabulimia. La AN es igual de frecuente que en las personas sin diabetes, pero el riesgo de hipoglucemias, cetosis por ayuno y cetoacidosis (CAD), desnutrición y complicaciones metabólicas es mayor. La BN y el TA en la DM1 es algo diferente; los atracones se caracterizan principalmente por un consumo excesivo y sin control de carbohidratos que favorecen la hiperglucemia, pero también la cetosis, siendo ésta última la que lleva a la pérdida de peso. El riesgo de hipoglucemia en estos casos es importante cuando se usan “mega dosis” de insulina para compensar los atracones. Sin embargo, el TCA más frecuente es la diabulimia. El término “diabulimia” resulta de la combinación de dos palabras, diabetes y bulimia y se caracteriza por la restricción u omisión deliberada de la administración de insulina para conseguir perder peso. Este trastorno no está reconocido en el manual DSM-5 aunque su prevalencia sobre todo en mujeres es muy elevado. La omisión de insulina produce una hiperglucemia y un estado cetogénico mantenido que hace perder peso, pero el riesgo de hipo e hiperglucemias, de CAD y de aparición precoz de las complicaciones crónicas es muy elevado.
Aunque no hay consenso en los criterios diagnósticos de T1DE, en 2020 The Royal College of Psychiatrists de Inglaterra y Gales propuso los 3 siguientes:
- Un intenso miedo a ganar peso y/o a aumentar la insulina
- La restricción u omisión de la administración de insulina y/o restricción de carbohidratos.
- Los dos criterios anteriores junto con una importante repercusión en la salud física y mental.
Las herramientas diagnósticas para evaluación de los TCA no están diseñadas específicamente para pacientes con diabetes y pueden subestimar/sobrestimar los problemas alimentarios. Durante los últimos años se han buscado herramientas útiles y validadas para la detección precoz de los T1DE.
El cuestionario “The Diabetes Eating Problem Survey (DEPS-R)» o la versión en español “Encuesta de Problemas alimentarios en Diabetes resumida (EPAD-R)» es una prueba rápida y validada para el despistaje de estos pacientes. No está claro a quién y cuándo se deben pasar estos cuestionarios. La American Diabetes Association (ADA) en 2023 lo recomienda en aquellos pacientes con hiperglucemia mantenida junto con una pérdida de peso no explicada, pero otras guías lo indican en el proceso de transición de pediatría a adultos junto con la elaboración de un programa educativo adaptado y coordinado.
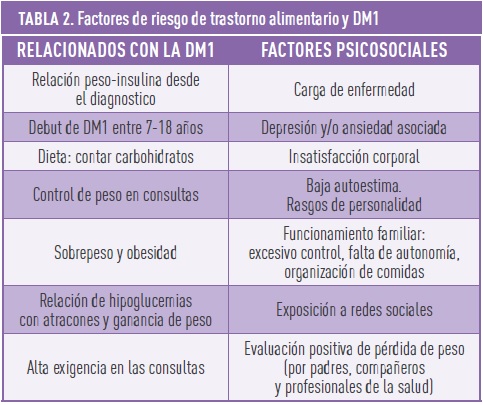
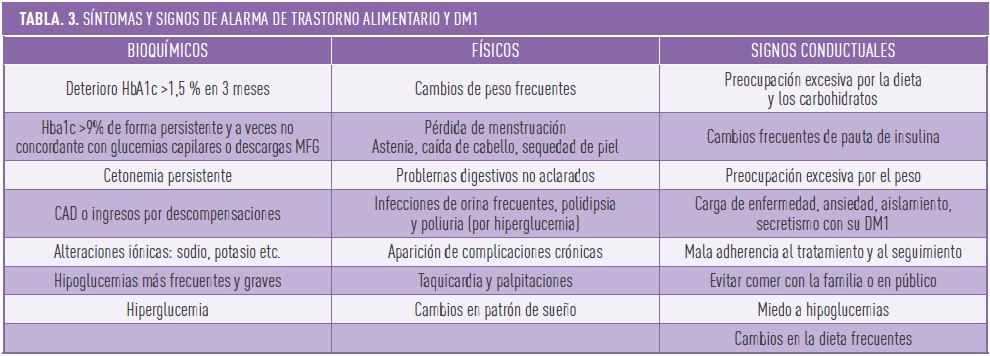
Dado que tenemos aún escasas herramientas de cribado de T1DE, debemos vigilar los principales factores de riesgo conocidos en nuestros pacientes (Tabla 2) y estar atentos a los signos de alarma que nos pueden hacer sospechar la presencia de algún trastorno de alimentación asociado (Tabla 3). Cuando hablamos específicamente de diabulimia, es decir de omisión de administración de insulina, existen otros signos de alerta que están relacionados con el mal uso de la insulina (no cebar la pluma, inyectarse en zonas de lipodistrofia o sobre la ropa, “estropear” la insulina para que pierda sus propiedades…), con un uso incorrecto de las bombas de insulina o ISCI (cambiar dosis programadas, introducir menos carbohidratos de los ingeridos para evitar corrección etc.) o con un uso inadecuado de los medidores de glucosa y cetonemia.
No debemos minimizar la diabulimia y los T1DE en general. Se sabe que su presencia aumenta y empeora las complicaciones micro y macrovasculares, incrementa el riesgo de complicaciones agudas (hipoglucemias graves, riesgo casi 3 veces mayor de CAD) y, por supuesto, empeora la salud mental y la calidad de vida. La tasa de mortalidad es casi 6 veces mayor y disminuye la esperanza de vida en 14 años en relación con personas con DM1 sin TCA. Dado la gravedad y el impacto que tienen sobre la salud de nuestros pacientes, debemos incidir en su prevención. Para ello, debemos buscar una atención centrada en la persona, ofertando un tratamiento individualizado con programas educativos estructurados, donde el paciente y también su familia, se involucren, opinen y tomen decisiones de forma coordinada con el equipo de diabetes. Los profesionales debemos estar formados no solo en DM1 sino en los TCA para evitar mensajes contradictorios y usar un lenguaje positivo y motivador, siendo flexibles, adaptándonos a las necesidades de nuestros pacientes, sin culpabilizar y poniendo el foco en la salud y en los hábitos de vida saludables.
Ante la sospecha de T1DE, el paciente debe ser evaluado por un equipo de Salud Mental (SM), quien confirmará el diagnóstico y trabajará de forma coordinada con el equipo de diabetes. El diabetólogo y la educadora deben adaptar el seguimiento e individualizar el tratamiento a la nueva situación de riesgo, incorporando:
- La valoración nutricional con una encuesta dietética más exhaustiva teniendo en cuenta el número de comidas, con quién comen, horarios, distribución de nutrientes y su relación con los carbohidratos.
- Supervisar la administración de insulina, detectar el uso de mega dosis compensatorias, evolución de HbA1c de los últimos meses, observar cambios de parámetros de glucometría, etc.
El tratamiento de pacientes con T1DE debe ser un tratamiento integral, basado en un modelo de atención compartida, individualizado, y evaluando por lo tanto la carga de enfermedad y otros problemas psicosociales asociados (Figura 1). La educación nutricional es la herramienta terapéutica fundamental para conseguir normalizar la conducta alimentaria y debe ser parte del tratamiento integral. Sus objetivos principales son: normalizar patrones y conductas alimentarias evitando restricciones, conseguir un estado nutricional adecuado y aumentar conocimientos nutricionales despejando dudas, erradicando mitos y bulos. Tenemos que buscar una meta compartida de peso saludable y una dieta equilibrada, intentando un equilibrio entre un enfoque intuitivo y flexible con la necesidad de contar carbohidratos para el control de la diabetes. Según evolución y gravedad del trastorno alimentario, algunos pacientes necesitarán un tratamiento intensivo y coordinado, que podrá ser en el hospital de día de diabetes y de salud mental o cuando el riesgo para la salud sea muy grave, precisará de una hospitalización completa.
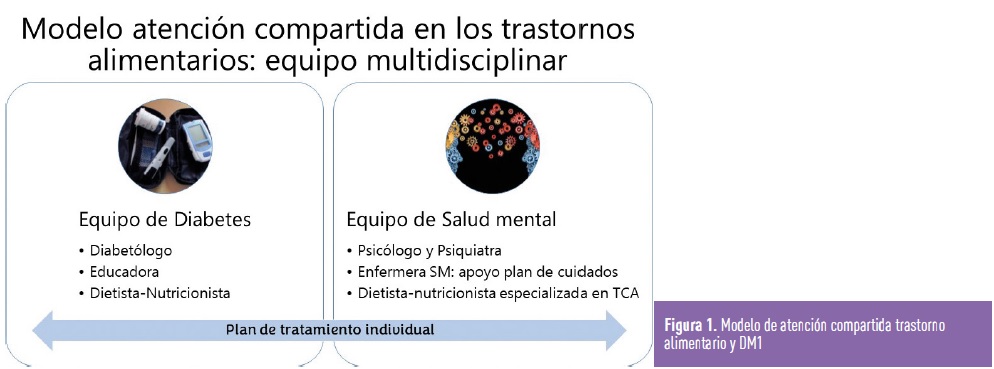
El tratamiento intensivo necesita una coordinación de cuidados entre el equipo de diabetes y el equipo de Salud Mental () (SM) y consta de 2 partes: el proceso de reinsulinización y el de realimentación.
La reinsulinización es el proceso de reintroducción de la insulina. Genera más angustia y ansiedad que la propia realimentación. Se debe comenzar con una pauta no negociable de insulina bolo-basal y debe estar supervisada su administración. Se recomienza comenzar para evitar cetosis, alteraciones electrolíticas e hipoglucemia con bajas dosis de insulina basal (por ej. 0,2-0,3 UI/Kg, 10UI) y una dosis fija insulina rápida (al menos 2UI/comida).
La realimentación es el proceso de reintroducción de alimentos y carbohidratos que debe hacerse junto con la reinsulinización. Se recomienda iniciar dietas con 150 g/día de carbohidratos, incluyendo media ración en cada comida progresando a una completa por comida cada 2 o 3 días.
El tratamiento de los T1DE es extremadamente complejo y no hay consenso sobre el mejor enfoque. Los pacientes T1DE tienen más probabilidades de abandonarlo debido a que la terapia ambulatoria convencional de su TCA tiene peores resultados. Existe consenso en la importancia de un equipo interdisciplinar (diabetólogos, salud mental, nutricionista, educadora, etc.), con una atención individualizada que aborde de forma global ambas patologías con el objetivo de lograr un peso saludable y procurando un control glucémico aceptable (con objetivos más laxos) que disminuya el riesgo de complicaciones graves. Es imprescindible la reeducación de hábitos dietéticos promoviendo comidas variadas y evitando restricciones, buscar programas de ejercicio físico adecuados, evitar la culpabilización. Y desde SM, realizar intervenciones que busquen aumentar la autoestima, la aceptación del cuerpo, además de las intervenciones familiares.
Queda mucho por conocer sobre el uso de tecnología en T1DE. LA tecnología en diabetes aumenta los conocimientos, la gestión de la propia enfermedad, el autocuidado, la calidad de vida y mejora el control glucémico y por eso podría ser útil en la prevención de estos trastornos. Por otro lado, podría ayudar a los profesionales a su detección al observar con más facilidad la propia omisión de insulina, las posibles transgresiones dietéticas o la presencia de una importante variabilidad glucémica que pueda hacer sospechar un T1DE. En relación con el tratamiento, la monitorización de cetonemia sería de interés, al igual que la supervisión de las dosis insulina administradas mediante Smart-pens (bolígrafos inteligentes o conectados) o los propios infusores de insulina ya que facilitarían adaptar mejor la insulina y dar mayor flexibilidad en las comidas.
Para concluir, la diabulimia es un trastorno alimentario frecuente y que, a pesar de sus graves consecuencias, no ha sido reconocido como enfermedad en DSM-5. Esto favorece que sea infradiagnosticado y no tratado por los propios profesionales implicados en el manejo de la diabetes. La asociación de TCA y diabetes dificulta el tratamiento en todas las áreas, incrementa la morbimortalidad y disminuye la calidad de vida de nuestros pacientes. Necesitamos estudios metodológicamente más sólidos para abordar la creciente necesidad de una vía de tratamiento clara y especializada promoviendo así la mejora de complicaciones agudas y el pronóstico a largo plazo.
BIBLIOGRAFÍA
- Galmiche M, Déchelotte P, Lambert G, Tavolacci MP. Prevalence of eating disorders over the 2000–2018 period: a systematic literature review. Am J Clin Nutr 2019;109:1402-13. DOI: 10.1093/ajcn/nqy342
- C. Gómez Candela et al. Guía para la prevención de los Trastornos de la Conducta Alimentaria (TCA). Nutr Hosp 2022;39(N.º Extra 2):3-7
- Asociación Americana de Psiquiatría, Guía de consulta de los criterios diagnósticos del DSM 5. Arlington, VA, Asociación Americana de Psiquiatría, 2013. ISBN 978-0-89042-551-0
- Banting, R., & Randle-Phillips, C. (2018). A systematic review of psychological interventions for comorbid type 1 diabetes mellitus and eating disorders. Diabetes Manag 2018; 8(1): 001–18
- ElSayed NA, Aleppo G, Aroda VR, et al. 5. Facilitating Positive Health Behaviors and Well-being to Improve Health Outcomes: Standards of Care in Diabetes-2023. Diabetes Care. 2023;46(Supple 1):S68-S96. doi:10.2337/dc23-S005
- Queensland Diabetes Clinical Network. Disordered Eating and Eating Disorders in Children, Adolescents and Adults with Type 1. Queensland Health. Diabetes – August 2022
- Guidance on Recognising and Managing Medical Emergencies in Eating Disorders , The Royal College of Psychiatrists, May 2022
- Goddard G, Oxlad M. Caring for individuals with Type 1 Diabetes Mellitus who restrict and omit insulin for weight control: Evidence-based guidance for healthcare professionals. Diabetes Res Clin Pract. 2022;185:109783. doi:10.1016/j.diabres.2022.109783
- Gibbings NK, Kurdyak PA, Colton PA, Shah BR. Diabetic Ketoacidosis and Mortality in People With Type 1 Diabetes and Eating Disorders. Diabetes Care. 2021;44(8):1783-1787. doi:10.2337/dc21-0517
- Sancanuto C, Jiménez-Rodríguez D, Tébar FJ, Hernández-Morante JJ. Translation and validation of the Diabetes Eating Problem Survey to screen eating disorders in patients with type-1 diabetes mellitus. Traducción y validación de un cuestionario para la detección de trastornos del comportamiento alimentario en pacientes con diabetes mellitus. Med Clin (Barc). 2017;148(12):548-554. doi:10.1016/j.medcli.2016.12.035







