Aunque las formas más comunes de diabetes mellitus son la diabetes tipo 1 y la diabetes tipo 2, existen otras formas de diabetes, entre las que se encuentran las diabetes monogénicas, clásicamente conocidas como diabetes tipo MODY. Confirmar un diagnóstico correcto de diabetes monogénica puede ayudar a personalizar el tratamiento farmacológico del paciente, su seguimiento clínico posterior, permite realizar un consejo genético adecuado para sus familiares, y también facilita un mejor conocimiento de los mecanismos relacionados con la hiperglucemia.
A diferencia de lo que ocurre en la diabetes tipo 1 y en la diabetes tipo 2 (consideradas como enfermedades poligénicas en las que el riesgo se ve afectado por características genéticas de muchos genes), en las diabetes monogénicas, la hiperglucemia es consecuencia de alteraciones que afectan a un único gen. Se han descrito formas excepcionalmente infrecuentes de diabetes monogénicas relacionadas con procesos autoinmunes, con la acción periférica de la insulina y con lipodistrofias, sin embargo, en este documento nos centraremos en las diabetes monogénicas que afectan al correcto funcionamiento de la célula beta (célula secretora de la insulina a nivel del páncreas), clásicamente conocidas como maturity-onset diabetes of the young o MODY.
LA PRINCIPAL LIMITACIÓN PARA SU DIAGNÓSTICO ES LA FALTA DE SOSPECHA CLÍNICA
Resulta de gran importancia destacar, como veremos más adelante, que existen diferentes tipos de diabetes tipo MODY, con sus características clínicas y de respuesta al tratamiento diferenciales, y que la principal limitación para el diagnóstico de este tipo de diabetes es la falta de sospecha clínica o su desconocimiento por parte del profesional que atiende a la persona con diabetes.
¿Cuál es la frecuencia de las diabetes monogénicas?
Aunque no existen estudios realizados en la población general (con y sin diabetes) que nos permitan saber con certeza, cuál es la frecuencia de las diabetes monogénicas en la población, los estudios más actuales realizados en Europa, Estados Unidos de América y Australia permiten estimar que, aproximadamente, un 0,5% de todas las personas con diabetes (1 de cada 200) presenta alguna forma de diabetes monogénica. Este número es mayor, alcanzando entre el 1 y 2%, cuando los estudios hacen referencia a la población pediátrica con diabetes (1 de cada 100 a 1 de cada 50 niños con diabetes). Por otra parte, cuando los estudios genéticos que permiten confirmar el diagnóstico de diabetes monogénica se realizan en un contexto de práctica clínica asistencial (no con un objetivo de investigación) y siguiendo una serie de criterios clínicos y de laboratorio, como el diagnóstico de diabetes con una edad inferior a los 30 años, la ausencia de autoinmunidad frente a la célula beta y la persistencia de secreción de insulina tras varios años desde el diagnóstico, el porcentaje puede aumentar hasta más del 20% de las personas con diabetes estudiadas (1 de cada 5) (1-4).
¿Cuándo deberíamos sospechar la posibilidad de una diabetes monogénica?
Como se comentó previamente, la principal barrera para el diagnóstico de los pacientes con diabetes monogénicas es la falta de sospecha clínica o su desconocimiento, por lo que una descripción adecuada de las características clínicas de sospecha debería servir de ayuda.
A continuación, describimos 4 perfiles clínicos, fácilmente identificables, sugerentes de diabetes monogénicas.
Pacientes con diabetes diagnosticados antes de los 6 a 12 meses de edad. Son muy infrecuentes, pero desde el punto de vista clínico son fácilmente reconocibles, y se considera un perfil clínico en el que el estudio genético es obligado. El término utilizado más habitualmente para designarlas es el de diabetes neonatales porque inicialmente se relacionaron con diabetes de inicio en los primeros 30 a 50 días de vida. Es importante destacar que hasta los 6 meses de edad es más frecuente que la diabetes sea debida a una alteración monogénica que a un origen autoinmune. Por otra parte, aunque se trata de un perfil clínico que se desarrolla en la edad pediátrica, debe tenerse en cuenta que algunas de estas personas con diabetes podrían llegar a la transición a la vida adulta sin el diagnóstico o el tratamiento adecuados (5-6).

Pacientes con diabetes asociada a otras enfermedades extrapancreáticas, como sordera o quistes renales. Al igual que en el cuadro clínico previo, se trata de formas de diabetes muy infrecuentes y, en este caso, sería la aparición de las enfermedades extrapancreáticas las que deberían hacer sospechar la posibilidad de una diabetes monogénica. En el síndrome de quistes renales y diabetes es fundamental comprender que las manifestaciones renales (la más habitual es la presencia de poliquistosis renal) suelen preceder al diagnóstico de diabetes, e incluso puede ser detectada en la ecografía intraútero. Así pues, estos pacientes suelen realizar su seguimiento clínico en los Servicios de Nefrología y será la aparición de hiperglucemia la que nos debe hacer pensar en su diagnóstico y estudio genético. Otras manifestaciones clínicas descritas son los quistes en el epidídimo y las malformaciones uterinas. Por otra parte, la coexistencia de diabetes y sordera debería hacernos sospechar el síndrome conocido como MIDD (maternally inherited deafness and diabetes) que puede estar relacionada con la presencia de alteraciones a nivel del ADN mitocondrial (se trata de un material genético trasmitido a la descendencia sólo por la madre, de ahí su herencia de transmisión materna). Los pacientes afectados por esta alteración genética pueden presentar también miopatía (dolores musculares) o distrofia macular (alteración visual) (5).
ES IMPORTANTE DESTACAR QUE HASTA LOS 6 MESES DE EDAD ES MÁS FRECUENTE QUE LA DIABETES SEA DEBIDA A UNA ALTERACIÓN MONOGÉNICA QUE A UN ORIGEN AUTOINMUNE
Pacientes con diabetes o hiperglucemia leve y estable desde el nacimiento. La presencia de una hiperglucemia leve (100-125 mg/dL) en ayunas que se mantiene estable desde el nacimiento también podría deberse a una diabetes monogénica. En estos casos, la dificultad más importante para establecer la sospecha clínica se debe a que, el carácter asintomático de este trastorno puede hacer que el diagnóstico de diabetes (o de hiperglucemia) se retrase hasta edades en las que podría confundirse con la presencia de diabetes tipo 2 y, por otra parte, aunque se trate de una enfermedad monogénica y hereditaria, la ausencia de clínica y de complicaciones asociadas puede hacer que el paciente desconozca la presencia de diabetes en sus familiares directos. Al tratarse de una hiperglucemia leve que se mantiene estable desde el nacimiento, el hecho de objetivar valores normales de glucosa antes del momento de la valoración nos permitiría descartar el diagnóstico sin necesidad de realizar el estudio genético (5-7).
Pacientes en edad pediátrica o adultos jóvenes (menos de 30 años en el momento del diagnóstico) que presentan características clínicas atípicas para la diabetes tipo 1 y la diabetes tipo 2. En este caso resulta imprescindible incluir características clínicas o de laboratorio que aumenten la probabilidad de que el paciente sometido al estudio genético tenga un resultado positivo. Además de la edad en el momento del diagnóstico, existen dos características de laboratorio que serán habitualmente evaluadas. Es importante que la autoinmunidad frente a la célula beta sea correctamente evaluada, incluyendo las determinaciones de los anticuerpos más importantes (anti GAD, IA2 y ZnT8A). Un resultado positivo de la autoinmunidad frente a la célula beta orientará a un diagnóstico de diabetes tipo 1, aunque la presentación clínica no sea típica. El segundo dato analítico de gran ayuda para valorar la posibilidad de diabetes monogénicas es la determinación del péptido C, que permite evaluar la reserva de insulina en la célula beta. Valores de péptido C estimulado (determinado sin realizar ayuno, tras estímulo con glucagón o tras realizar un test de comida mixta) bajos son muy sugerentes de diabetes tipo 1 (5,7,9).

¿Qué tipo de prueba es necesario realizar para confirmar el diagnóstico?
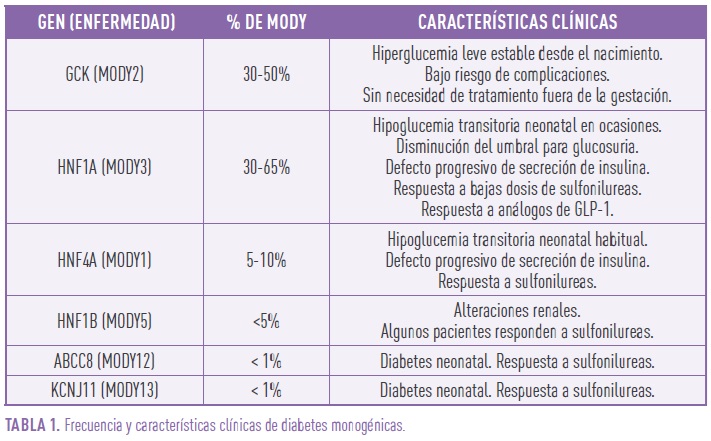
Como comentamos previamente, se han descrito múltiples variantes genéticas relacionadas con diabetes monogénicas asociadas a disfunción de la célula beta, sin embargo, la mayoría son excepcionales y sólo 4 de ellas (GCK, HNF1A, HNF4A, HNF1B) suponen más de un 1% del total de diabetes monogénicas. Al tratarse de una enfermedad genética, el diagnóstico de confirmación exigirá la demostración de una alteración en el gen estudiado, para lo que será suficiente con una extracción de sangre similar a las realizadas para cualquier determinación analítica.
Existen diferentes aproximaciones al estudio genético, y su selección puede depender de las características clínicas del paciente con sospecha de diabetes monogénica.
Estudio de un gen aislado. La presencia de diabetes o hiperglucemia leve y estable desde el nacimiento sugiere la presencia de mutaciones en GCK. La presencia de diabetes y sordera de herencia materna se asocia, en la mayoría de los casos, a una mutación puntual en el gen mitocondrial MT-TL1 y, en unos pocos casos a mutaciones puntuales de los genes mitocondriales MT-TE y MT-TK. Finalmente, el síndrome de quistes renales y diabetes se relaciona con mutaciones en HNF1B. Estas alteraciones clínicas no se asocian a otras alteraciones genéticas descritas por lo que, en estos casos, la secuenciación aislada del gen podría ser adecuada.
Estudio mediante paneles genéticos. Permiten estudiar de manera simultánea un número determinado de genes previamente seleccionados por su relación con el cuadro clínico estudiado. Este tipo de estudio genético será de gran utilidad cuando las características clínicas del paciente pueden ser debidas a alteraciones genéticas en diferentes genes (por ejemplo, en HNF1A o HNF4A). No podemos obviar que, al aumentar el número de genes estudiados es más probable la detección de alteraciones genéticas con significado incierto y que no siempre tienen por qué justificar el cuadro clínico que presenta el paciente.
LOS OBJETIVOS FUNDAMENTALES DE LA CONFIRMACIÓN GENÉTICA SON OFRECER A LA PERSONA CON DIABETES UN TRATAMIENTO FARMACOLÓGICO Y UN SEGUIMIENTO PERSONALIZADOS
¿Qué recomendaciones podría recibir en caso de presentar una diabetes monogénica?
Como comentamos con anterioridad, los objetivos fundamentales de la confirmación genética son ofrecer a la persona con diabetes un tratamiento farmacológico y un seguimiento personalizados.
Diabetes monogénica asociada a mutaciones en GCK (MODY-2). Las evidencias disponibles indican que su control glucémico no muestra diferencias relevantes cuando estos pacientes se encuentran en tratamiento con fármacos antidiabéticos no insulínicos o con insulina, y tras su retirada. Así pues, la recomendación general ante la confirmación genética de diabetes monogénica asociada a mutaciones en GCK será la retirada del tratamiento farmacológico con reevaluación posterior del paciente. Con relación al seguimiento clínico, los pacientes con diabetes monogénica asociada a mutaciones en GCK tienen un muy bajo riesgo de complicaciones asociadas a la hiperglucemia por lo que, el cribado de las mismas debería individualizarse. El aspecto más importante o con mayor debate en el manejo del paciente con diabetes monogénica asociada a mutaciones en GCK hace referencia al manejo de las pacientes durante la gestación, y en ese caso, el manejo debe individualizarse (5,7).
Diabetes monogénica asociada a mutaciones en HNF1A (MODY-3) y HNF4A (MODY-1). Se ha descrito que los pacientes con diabetes monogénica asociada a mutaciones en HNF1A y en HNF4A presentan una excelente respuesta al tratamiento con sulfonilureas o glinidas y la confirmación genética aconsejaría intentar realizar el cambio de tratamiento. A pesar de eso, no todos los pacientes consiguen un adecuado control glucémico con sulfonilureas. Con relación al seguimiento clínico asociado al riesgo de desarrollo de complicaciones crónicas, los pacientes con diabetes monogénica asociada a mutaciones en HNF1A y HNF4A presentan un riesgo equivalente al objetivado en pacientes con otros tipos de diabetes por lo que las recomendaciones de seguimiento y control de comorbilidades y factores de riesgo cardiovascular no deberían ser diferentes de las aplicadas a otros pacientes con diabetes (5).

Pacientes con diabetes monogénica asociada a mutaciones en HNF1B (MODY-5). Estos pacientes pueden ser sensibles al tratamiento con sulfonilureas, aunque en ningún caso los resultados serán los esperados para pacientes con MODY-3. De esta manera, el tratamiento con sulfonilureas podría ser una opción terapéutica, pero después, el tratamiento tendrá que adaptarse a la respuesta individual del paciente (10).
Pacientes con diabetes monogénica asociada a mutaciones en KCNJ11 y ABCC8. Se trata de un perfil clínico que se desarrolla en la edad pediátrica y se ha demostrado la respuesta adecuada de estos pacientes al tratamiento con sulfonilureas, siendo ésta la opción terapéutica de elección (6).
Resto de pacientes con diabetes monogénica (asociada a APPL1, BLK, CEL, INS, KLF11, NEUROD1, PAX4 y PDX1). Debido a su baja prevalencia, no existen recomendaciones específicas de cara a su tratamiento farmacológico o seguimiento clínico.
Resumen:
Como conclusiones, no podemos olvidar que existen otros tipos de diabetes, más allá de la diabetes tipo 1 y de la diabetes tipo 2, y que un correcto diagnóstico de una diabetes monogénica puede permitirnos retirar el tratamiento farmacológico y espaciar las pruebas de detección de complicaciones crónicas, como ocurre en las diabetes asociadas a mutaciones en GCK, o puede permitirnos suspender el tratamiento con insulina alcanzando un mejor control glucémico con una terapia farmacológica oral, como ocurre en las diabetes asociadas a mutaciones en HNF1A.
Bibliografía:
- Pihoker C, Gilliam LK, Ellard S, Dabelea D, Davis C, Dolan LM, et al. Prevalence, characteristics and clinical diagnosis of Maturity Onset Diabetes of the Young due to mutations in HNF1A, HNF4A, and Glucokinase: results from the SEARCH for diabetes in Youth. J Clin Endocrinol Metab. 2013; 98: 4055-62.
- Shepherd M, Shields B, Hammersley S, Hudson M, McDonald TJ, Colclough K, et al. Systematic population screening, using biomarkers and genetic testing, identifies 2.5% of the UK pediatric diabetes population with monogenic diabetes. Diabetes Care. 2016; 39: 1879-88.
- Rudland VL, Hinchcliffe M, Pinner J, Cole S, Mercorella B, Molyneaux L, et al. Identifying glucokinase monogenic diabetes in a multiethnic gestational diabetes mellitus cohort: new pregnancy screening criteria and utility of HbA1c. Diabetes Care. 2016; 39: 50-52.
- Shields BM, Shepherd M, Hudson M, McDonald TJ, Colclough K, Peters J, et al. Population-based assessment of a biomarker-based screening pathway to aid diagnosis of monogenic diabetes in Young-onset patients. Diabetes Care. 2017; 40: 1017–25.
- Murphy R1, Ellard S, Hattersley AT. Clinical implications of a molecular genetic classification of monogenic beta-cell diabetes. Nat Clin Pract Endocrinol Metab. 2008; 4: 200-13.
- Lemelman MB, Letourneau L, Greeley SAW. Neonatal Diabetes Mellitus: An Update on Diagnosis and Management. Clin Perinatol. 2018; 45: 41-59.
- Pinés Corrales PJ, López Garrido MP, Louhibi Rubio L, Aznar Rodríguez S, López Jiménez LM, Lamas Oliveira C, et al. Importance of clinical variables in the diagnosis of MODY2 and MODY3. Endocrinol Nutr. 2011; 58: 341-6.
- Steele AM, Shields BM, Wensley KJ, Colclough K, Ellard S, Hattersley AT. Prevalence of vascular complications among patients with glucokinase mutations and prolonged, mild hyperglycemia. JAMA. 2014; 311: 279-286.
- Jones AG, Hattersley AT. The clinical utility of C-peptide measurement in the care of patients with diabetes. Diabet Med. 2013; 30: 803-17.
- Carrillo E, Lomas A, Pinés PJ, Lamas C. Long-lasting response to oral therapy in a young male with monogenic diabetes as part of HNF1B-related disease. Endocrinol Diabetes Metab Case Rep. 2017. pii: 17-0052.







