Desde los tiempos más remotos, la tendencia natural de los profesionales de la Medicina que atienden pacientes es la de fundamentar sus actuaciones en la experiencia. Han tomado las decisiones según los resultados previos y adaptando a los tiempos que les ha tocado vivir. Evidentemente Galeno no podía pedir una radiografía ni en la actualidad se deberían aplicar sanguijuelas. Pero también sabemos que la experiencia no permite resolver todos los problemas y por ello se ha tenido que experimentar nuevas ideas y nuevas técnicas, con resultados dispares.
La evolución de la medicina ha venido de la mano de la evolución de la tecnología. Actualmente se disponen de máquinas capaces de aprender más rápido que los humanos, de cometer menos errores, de llegar a diagnósticos complejos, de predecir el futuro de la historia natural de la enfermedad, la eficacia de un tratamiento y en definitiva de tomar decisiones que ayudan enormemente a los pacientes.
El abordaje tradicional de la enfermedad diabética pasa por un diagnóstico basado en unos puntos de corte de la glucemia, un tratamiento que permita reducir la glucemia a los valores más bajos posibles (sin provocar hipoglucemias) para evitar la aparición de complicaciones específicas de la enfermedad. Para ello se han utilizado distintas familias farmacológicas con distinto protagonismo en los distintos mecanismos fisiopatológicos que pueden estar implicados en la enfermedad.
En las últimas décadas se ha revalorizado enormemente la imperiosa necesidad de un estilo de vida saludable y de la implicación del paciente en el control de su enfermedad. Gracias a este esquema se ha conseguido reducir la morbimortalidad de la enfermedad y mejorar la calidad de vida de los pacientes.
Pero actualmente tenemos la sensación que hemos llegado a un techo de cristal que no permite seguir avanzando en la batalla contra la enfermedad diabética… y es cuando se ha empezado a pensar distinto de la mano de la tecnología. Particularmente, creo que el cambio de paradigma se produjo cuando se dejó de poner a la glucemia en el centro del proceso y se empezó a pensar que el objetivo real no era un control glucémico sino evitar las complicaciones y mejorar la calidad de vida de los pacientes.
Y en este proceso están implicadas muchas más cosas que la glucemia y son distintas para cada paciente y cada momento de la evolución de la enfermedad. Ahí nació la Medicina Personalizada de Precisión (MPP) y en nuestro caso la aplicada a la diabetes mellitus (DM).
LA MPP NO SOLO TIENE EL POTENCIAL DE MEJORAR LOS RESULTADOS DE SALUD PARA LAS PERSONAS CON DM, SINO QUE TAMBIÉN PODRÍA TENER UN IMPACTO SIGNIFICATIVO EN LA REDUCCIÓN DE LOS COSTOS DE ATENCIÓN MÉDICA
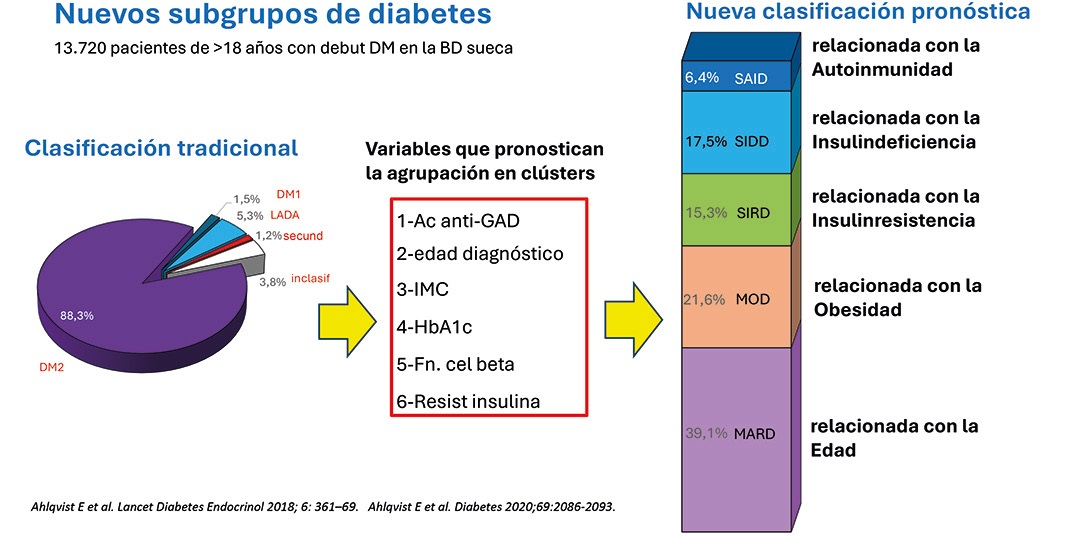
Probablemente el primer gran paso conceptual fue el del grupo escandinavo liderado por Emma Ahlqvist (1) que dejó de centrar el diagnóstico de la DM2 en un punto de corte de la glucemia y se preguntó ¿qué ocurriría a los pacientes?, ¿cuál sería el pronóstico de una persona a la que se acaba de diagnosticar una diabetes?, ¿todas tendrán la misma evolución?, ¿la misma respuesta al tratamiento?
Este grupo se ayudó de los avances en inteligencia artificial (IA) y de aprendizaje automático (Machine Learning). Mediante una técnica de clusterización pudo averiguar que en el momento del debut de la diabetes hay 5 variables predictoras muy importantes que van a cambiar el panorama futuro de cada paciente. A partir de los valores de la HbA1c, la edad en el debut, el índice de masa corporal (obesidad), la secreción de insulina por la célula beta pancreática y la resistencia periférica a la acción de la insulina (estas dos últimas medidas a partir de los valores del péptido C), se podían establecer 5 grupos de pacientes con distinta evolución, con distinta probabilidad de presentar alguna de las complicaciones, con distinta respuesta al tratamiento y en definitiva con distinto pronóstico. Y esto permitía intensificar algunas actuaciones preventivas y terapéuticas de forma distinta según cada persona.
La DM tipo 2 hasta ese momento había sido un cajón de sastre, donde cabían todas las formas de DM que no se podían clasificar en otros apartados. Ahora teníamos 5 patrones distintos de DM (las asociadas fuertemente a la inmunidad que se corresponderían con las clásicas diabetes tipo 1), las asociadas al déficit severo de secreción de insulina, a la resistencia a la acción de la insulina, a la obesidad o a la edad. En cada uno de ellos, el abordaje debe de ser distinto para minimizar el impacto de la enfermedad de una forma eficiente.
A partir de esta base de clasificación fenotípica se han desarrollado muchos más estudios complementarios. Así por ejemplo sabemos que la creación de estos grupos difiere según las etnias y pueden ser cambiantes en el tiempo (2) y por tanto es muy importante utilizar datos de nuestro entorno para poder tomar las mejores decisiones.
También sabemos de la importancia del genotipo que contribuye a modular los pronósticos basados en los fenotipos y a explicar los mecanismos por los que se producen estos resultados (3). Más recientemente se han publicado diversos estudios que demuestran la distinta eficacia y tolerancia de las distintas opciones de tratamiento farmacológico según el fenotipo y genotipo de los pacientes con DM.
Sin embargo, lo que está cambiando es el paradigma con el que estudiamos y entendemos la enfermedad y nuestra biología en general. Por un lado, los progresos en las ciencias ómicas, la epigenética o la microbiota nos ayudan a entender las causas y las variaciones entre individuos de muchos de los procesos biológicos. Por otro lado, la recopilación de billones de datos clínicos recogidos en los centros de salud de todo el mundo, junto con los avances tecnológicos en técnicas de aprendizaje automático, nos permiten analizar esta gran cantidad de datos para extraer de ellos conocimiento sobre la evolución de la diabetes.
Todo ello hace que nos replanteemos la enfermedad diabética. Las principales sociedades científicas han promulgado consensos y documentos específicos que reflexionan sobre este tema. Analizan las diferentes áreas en que puede ser de utilidad y establecen recomendaciones basadas en esta MPP (4).
En nuestro medio la MPP ha permitido establecer 7 trayectorias diferentes de la evolución de la DM según variables clínicas de uso habitual. Esto nos permite predecir si una persona es más propensa a presentar, por ejemplo, la enfermedad renal crónica y por tanto debería someterse con mayor frecuencia a estudios diagnósticos de esta patología y probablemente estaría justificado el uso de medidas preventivas incluso farmacológicas (5).
“SI BUSCAS RESULTADOS DISTINTOS NO HAGAS SIEMPRE LO MISMO” ALBERT EINSTEIN
Recientemente, también en España, se ha puesto en marcha un estudio que pretende cambiar el paradigma del abordaje de la DM desde el momento del debut de la enfermedad (estudio Copernican). Su finalidad es identificar desde el inicio los diferentes clusters en función de los diferentes pronósticos, de la aparición de complicaciones y de la distinta respuesta a las distintas opciones terapéuticas.
Otro estudio que se enmarca dentro de la estrategia IMPACT del Ministerio de Sanidad también intenta identificar alteraciones genómicas principalmente en los grupos extremos de pacientes en el debut de la DM.
Cuando estén completados estos y otros estudios similares, tendremos un perfil mucho más preciso de las personas con diabetes de nuestro entorno, podremos predecir mejor cual va a ser su pronóstico y por tanto podremos aplicar medidas preventivas y curativas con mayor eficacia y menos riesgo.
Otro de los grandes avances de la IA en el campo de la medicina y la diabetes es el uso de grandes bases de datos (Bigdata) (6) y de las bases de datos sintéticas. Gran parte de la evidencia científica que tenemos en la actualidad proviene de los resultados de los ensayos clínicos, con unas condiciones de entrada en el estudio muy restringidas. Aunque la validez interna de los resultados es incuestionable, su aplicabilidad (validez externa) suele ser muy reducida, porque la mayoría de los pacientes no cumplirían con las condiciones de inclusión de ensayo. A estos pacientes les aplicamos las conclusiones de estudios en los que ellos no hubieran podido entrar. Esto es especialmente cierto en algunos grupos de pacientes como los más ancianos o si existen comorbilidades asociadas (como enfermedad mental o insuficiencia renal crónica).
Para saber cómo actuar en esta gran cantidad de paciente, nos basamos en la experiencia de grandes bases de datos con una enorme cantidad de pacientes sin restricciones y larga evolución. En ellos sabemos que ha ocurrido y por tanto podemos intentar predecir qué ocurrirá en pacientes de características muy similares. Estos datos pueden usarse para desarrollar modelos de riesgo personalizados y para identificar nuevos objetivos terapéuticos y orientar las actuaciones preventivas y terapéuticas.
En ocasiones, a partir de la información de los Bigdata, se trabaja con simulaciones de los pacientes y se construye una base de datos de pacientes no reales, que no existen (Bases de Datos Sintéticas) (7), pero que tienen el mismo comportamiento que los que sí existen. Con ello, además de preservar datos confidenciales, podemos establecer diferentes análisis basados en las simulaciones minimizando los riesgos que supone trabajar con datos reales.
Un caso más específico seria trabajar con los denominados “gemelos digitales” o “pacientes artificiales” que sería clones imaginarios de pacientes reales (8). Con ellos podemos testar distintas opciones terapéuticas, tanto farmacológicas como de estilos de vida, sin riesgo para los pacientes.
Estas tecnologías ya se están aplicando en la actualidad.
Es importante destacar que la MPP no solo tiene el potencial de mejorar los resultados de salud para las personas con DM, sino que también podría tener un impacto significativo en la reducción de los costos de atención médica. Al enfocarse en las intervenciones más efectivas para cada paciente, la MPP podría ayudar a reducir el uso de medicamentos y hospitalizaciones innecesarias.
El futuro de la MPP aplicado a la diabetes es muy esperanzador (9). Tanto conceptualmente como tecnológicamente estamos en un camino nuevo, extraordinariamente ilusionante. Pero es importante tener en cuenta que la MPP no es una solución única para todos los problemas de la DM. Otro aspecto a tener en cuenta será el plan de desarrollo e implantación de la MPP en los distintos sistemas de salud y las dificultades que ello comporta. Se necesita un enfoque equilibrado que combine la MPP con los enfoques tradicionales para garantizar que todas las personas con DM tengan acceso a una atención de la más alta calidad posible.
Conclusiones
- La MPP tiene el potencial de transformar el manejo de la DM al proporcionar estrategias de diagnóstico, tratamiento y prevención más precisas y efectivas.
- Sin embargo, es importante abordar los retos y desafíos de la implementación de la MPP, así como las consideraciones éticas y sociales relacionadas con su uso.
- La investigación continua y la colaboración entre científicos, médicos, pacientes y responsables políticos serán esenciales para garantizar que la MPP se utilice de manera responsable y equitativa para mejorar la salud de las personas con DM y proporcionarles la mejora atención posible en cada momento.
Bibliografía
- Ahlqvist E, Storm P, Käräjämäki A, et al. Novel subgroups of adult-onset diabetes and their association with outcomes: a data-driven cluster analysis of six variables. Lancet Diabetes Endocrinol 2018; 6(5): 361-369
- Udler MS, McCarthy MI, Florez JC, et al. Genetic Risk Scores for Diabetes Diagnosis and Precision Medicine. Endocr Rev 2019; 40(6): 1500-1520
- Herder C, Roden M.: A novel diabetes typology: towards precision diabetology from pathogenesis to treatment. Diabetologia 2022; 65 (11): 1770-1781.
- Chung WK, Erion K, Florez JC, et al. Precision Medicine in Diabetes: A Consensus Report from the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2020; 43 (7): 1617-1635.
- Manzini E, Vlacho B, Franch-Nadal J, et al.: Longitudinal deep learning clustering of Type 2 Diabetes Mellitus trajectories using routinely collected health records. J Biomed Inform [Internet]. 2022; 104218. https://linkinghub.elsevier.com/retrieve/pii/S1532046422002234
- de Mauro A, Greco M, Grimaldi M. What is big data? A consensual definition and a review of key research topics. In: AIP Conference Proceedings. American Institute of Physics Inc.; 2015. p. 97-104.
- Stolfi P, Valentini I, Palumbo MC, et al.: Potential predictors of type-2 diabetes risk: machine learning, synthetic data and wearable health devices. BMC Bioinformatics. 2020; 21(Suppl 17): 508. doi: 10.1186/s12859-020-03763-4.
- Shamanna P, Saboo B, Damodharan S, et al.: Reducing HbA1c in Type 2 Diabetes Using Digital Twin Technology-Enabled Precision Nutrition: A Retrospective Analysis. Diabetes Therapy. 2020; 11 (11): 2703-2714
- Drucker, DJ; Hollander, P.: Precision medicine in diabetes—a perspective on the future. Nature Medicine, 2021; 27 (10): 1183- 1193 https://www.nature.com/articles/s41574-022-00799-9







